越来越多证据表明,哮喘是由独特的分子机制调控的异质性疾病。在一项对严重程度各异的哮喘患者进行的横断面研究中,支气管内组织基因表达分析显示出3个主要患者群:辅助T细胞2(TH2 )-高,TH17-高和TH2/17-低。在单个患者样本中,TH2-高和TH17-高模式相互排斥,并且其基因标签呈负相关,且分别由白介素-13(IL-13)和IL-17A调控。


结果发现,与TH17-高和TH2/17-低哮喘组相比,TH2 -高哮喘组呼出气一氧化氮(FeNO)和痰嗜酸性粒细胞百分比显著增加(图1A和B)。
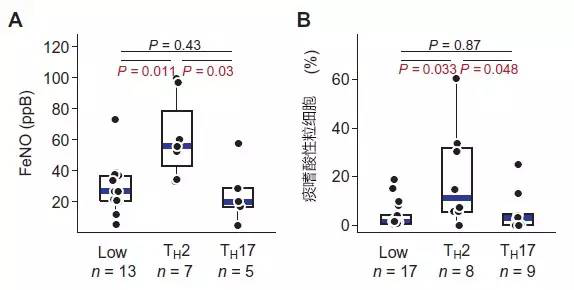
摘自:Choy DF, et al. Sci Transl Med. 2015;7(301):301ra129.
与TH2/17-低哮喘组相比,TH2-高哮喘组平均血嗜酸性粒细胞计数显著升高,TH17-高哮喘也有所升高,但与TH2/17-低哮喘组无统计学差异(图1C)。试验还对支气管活检黏膜固有层嗜酸性粒细胞计数进行了比较,与TH2/17-低哮喘组相比,TH2-高和TH17-高哮喘组嗜酸性粒细胞水平均显著升高(图1D)。对比TH2-高和TH2/17-低的哮喘,TH17-高的哮喘中血清骨膜蛋白中位水平最高(图1E)。

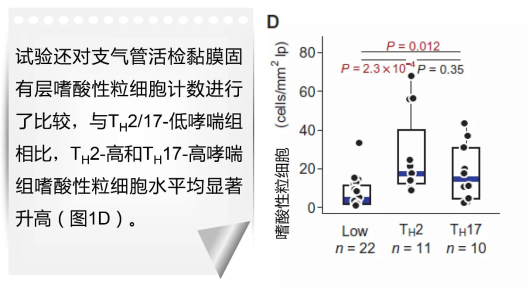

摘自:Choy DF, et al. Sci Transl Med. 2015;7(301):301ra129.
图1. TH2-高和TH17-高哮喘与生理性TH2水平/炎症嗜酸性粒细胞测量值水平升高均有关

根据嗜酸粒细胞性哮喘的迹象,即血嗜酸性粒细胞计数≥300μl或痰液嗜酸粒细胞百分数≥3,或活检固有层嗜酸粒细胞计数≥10/mm2,以及临床严重程度(英国胸科协会/苏格兰校际指南网络治疗步骤)对哮喘患者进行分类。如图2所示,TH17 -高哮喘只在糖皮质激素治疗的中重度哮喘中出现,不论轻、中、重度哮喘,TH2-高哮喘均在嗜酸性粒细胞高水平群体中出现。

摘自:Choy DF, et al. Sci Transl Med. 2015;7(301):301ra129.
图2.按临床嗜酸性粒细胞水平和哮喘严重程度划分的哮喘TH2/17分子表型比例

TH2和TH17在人类哮喘气道中存在相互排斥,体外抑制IL-13可以促进IL-17的产生。观察单独或合并阻断IL-4和IL-13,对过敏性哮喘小鼠模型TH17的影响。结果发现,所有的抗TH2的干预导致肺和淋巴结组织中IL17表达和CD4+IL-17+细胞的显著增加,特别是抗IL-4(图3)。

摘自:Choy DF, et al. Sci Transl Med. 2015;7(301):301ra129.
图3. 治疗阻断TH2细胞因子导致代偿性的TH17炎症

基于以上结果,观察单独或合并阻断IL-13/17的疗效,结果发现,与对照抗体或单独抗IL-17小鼠相比,单独抗IL-13或合并抗IL-13/抗IL-17小鼠的气道高反应性和粘液应答基因表达显著降低。接受双重抗IL-13/抗IL-17治疗小鼠的由单独抗IL-13导致的IL-17的增加和嗜中性粒细胞浸润可以被分别部分和完全消除。

IL-4和/或IL-13的拮抗会导致TH17细胞增加和肺部中性粒细胞炎症。尽管如此,IL-13和IL-17的拮抗可以保护小鼠避免患嗜酸粒细胞增多、粘液增生、气道高反应性并能消除中性粒细胞性炎症,这提示在同时具有TH2和TH17表型的人群中,针对两种途径的联合疗法可能会使治疗效果最大化。
参考文献:Choy DF, Hart KM, Borthwick LA, et al. TH2 and TH17 inflammatory pathways are reciprocally regulated in asthma. Sci Transl Med. 2015;7(301):301ra129.